进口保健食品市场准入的核心政策依据为《中华人民共和国食品安全法》第七十六条及《保健食品注册与备案管理办法》。其中,《食品安全法》明确:使用保健食品原料目录以外原料的保健食品、首次进口且非补充维生素 / 矿物质的保健食品需经国家市场监督管理总局注册,首次进口的补充维生素 / 矿物质类保健食品需备案,其他保健食品报省级监管部门备案,且进口产品需为出口国(地区)准许上市的产品。
保健食品注册是监管部门对产品安全性、保健功能、质量可控性进行系统评价审评,决定是否准予注册的审批过程;备案则是生产企业提交相关材料存档、公开、备查的过程。

二者核心区别如下:进口注册申请人与备案人均为境外生产厂商;适用范围上,进口注册针对首次进口的非维生素 / 矿物质类产品,备案针对首次进口的维生素 / 矿物质类产品;审批单位均为国家市场监督管理总局;流程周期上,注册需 3-5 年(含技术审评、现场审核等),备案需 6-12 个月(系统填报、资料补充等)。

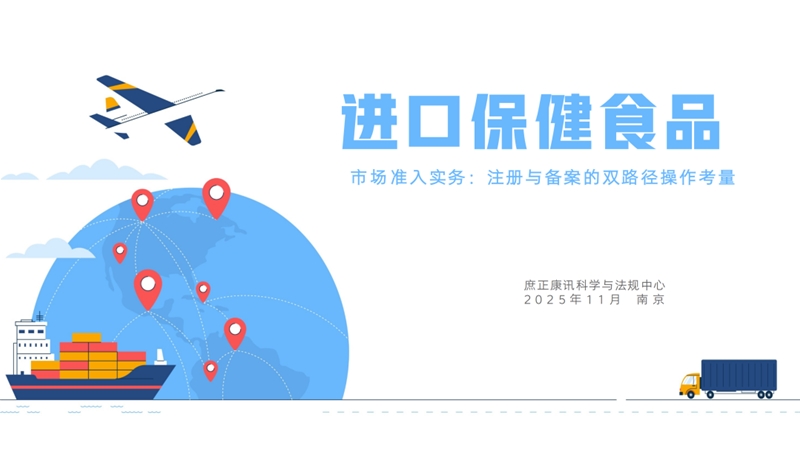
此外,《保健食品原料目录营养素补充剂(2023 年版)》包含 15 种维生素、8 种矿物质及 1 种宏量营养素(DHA 藻油);《功能原料目录》含 10 种原料(如辅酶 Q10、破壁灵芝孢子粉等)及对应保健功能;
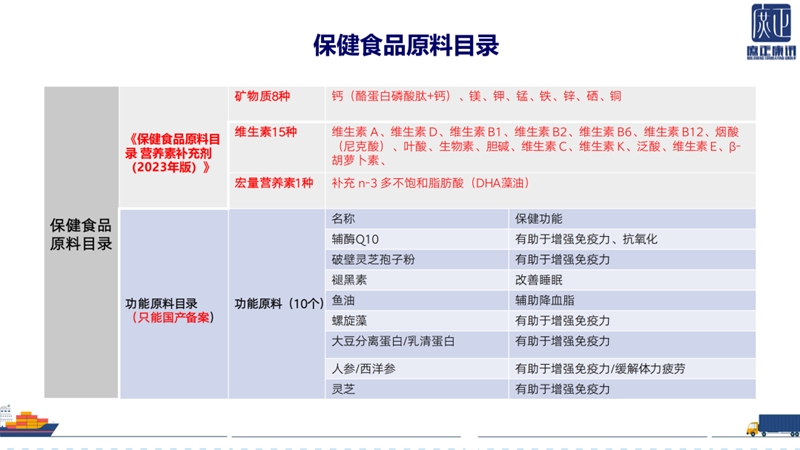
《允许保健食品声称的保健功能目录非营养素补充剂(2023 年版)》将 24 项功能分三类试验(13 项需动物 + 人体试验、7 项仅需动物试验、4 项仅需人体试验)。
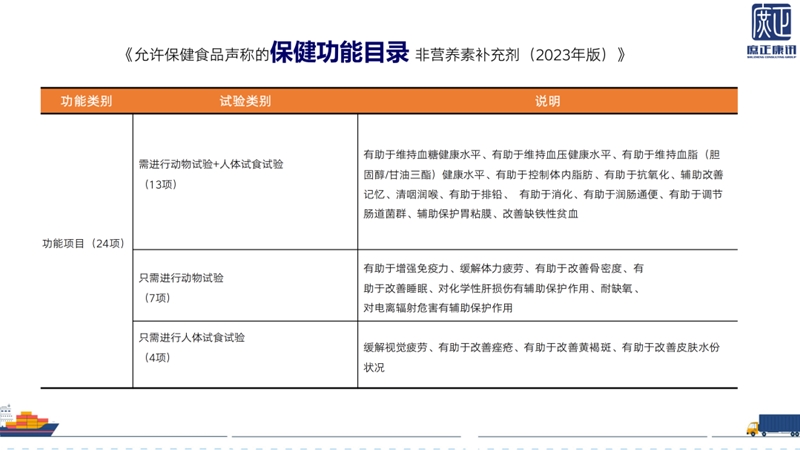
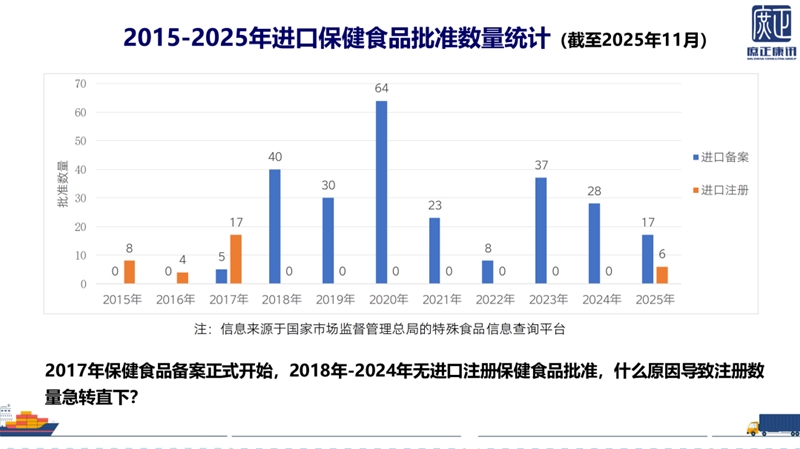
2015-2025 年进口保健食品批准数量统计显示,2017 年备案正式启动,2018-2024 年无进口注册产品批准,2025年目前已批准6款。
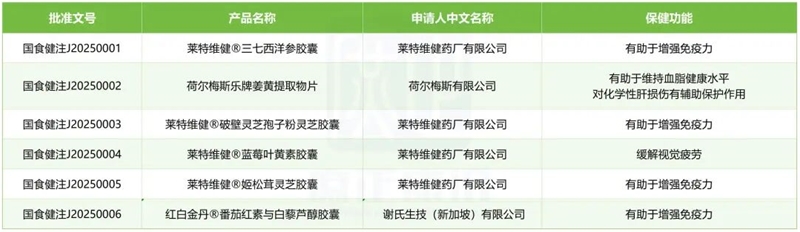
2025年,在国家市场监督管理总局特殊食品信息查询平台中搜索发现,共有6款进口保健食品获批,迎来自2018年后的首次破冰!6款获批产品来自3家企业,其中4款来自中国香港,1款来自印度尼西亚,一款来自新加坡。
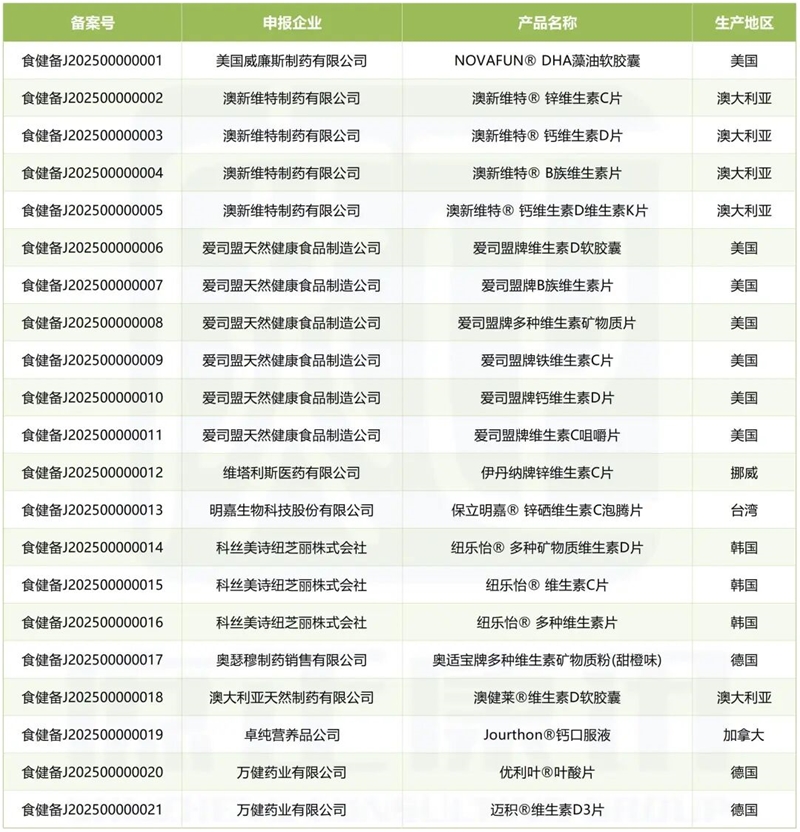
国家市场监督管理总局食品审评中心查询,截止目前,21款进口产品通过备案路径获得“蓝帽子”。
备案制周期短、成本低,适用于原料在目录内的标准化产品,需严守目录边界;注册制周期长、难度大,适用于创新或复杂配方产品;新功能注册针对高质量创新产品,可解决保健食品同质化问题,但成本高、周期长,企业需根据产品特性选择适配路径。
声明:转载此文是出于向母婴行业传递更多信息之目的。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。联系方式:168466559@qq.com



长按扫码 阅读原文


