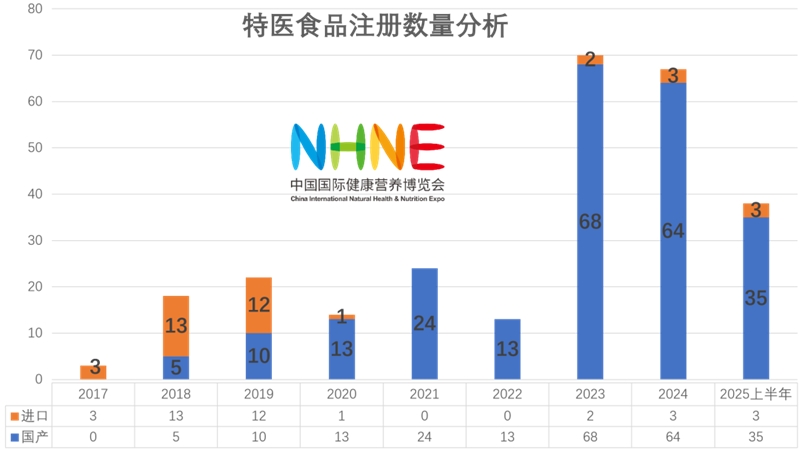
据国家市场监督管理总局特殊食品信息查询平台数据显示,截至2025年6月30日,新增特医食品获批38款(其中进口产品3款,国产35款),已获批特医食品数量增至269款(含已注销的5款)。NHNE将对所有获批的特医产品进行了统计汇总,并从多角度进行分析,供行业同仁了解和参考。
01
产品类型分析
2025年上半年获批的38款新产品中,青岛圣桐生产的特爱本佳和特爱丙佳这两款配方分别适用于苯丙酮尿症、甲基丙二酸血症和丙酸血症等罕见病患儿食用,打破了国内无罕见病配方的局面,对我国特医在罕见病领域的发展具有重要意义。获批产品中全营养配方食品数量最多,为14款,占获批总数的37%。其次为蛋白质(氨基酸)组件,为8款,占比21%,没有特定全营养类产品获批。从适用人群来看,2025年上半年获批数量最多的为适用于10岁以上人群的产品,共21款,占比55%。还首次推出了两款6~12月龄以及一款1~5岁适用的产品,针对人群年龄的划分更加精细。
截至2025年6月30日,国家市场监督管理总局发布通过注册的特医食品有269款(含已注销的5款),其中特医婴配食品67款,1岁以上特医食品202款,具体产品情况如下图所示:
特殊医学用途配方食品
(适用于1岁以上人群)
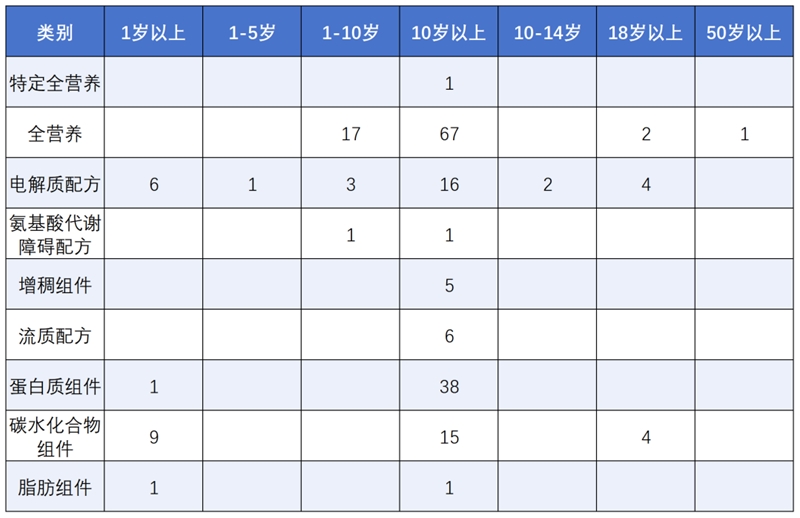
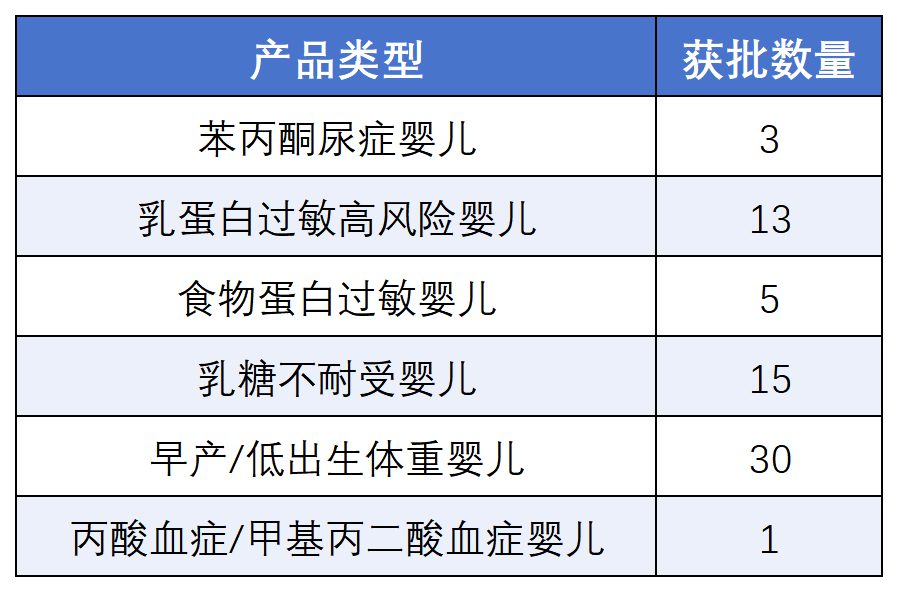
特殊医学用途婴儿配方食品
(适用于0月龄至12月龄儿童)
02
生产企业分析
2025年上半年新增获批企业13家,和氏乳业、美亚特医(中国香港)、汤臣倍健、鑫禾健各,白云山汉方、广西红山堂、广州力衡、华森制药、山东隆庆祥、时代特医、天源特医、中恩医药和中特食品,截至目前,共有78家企业获得特医食品注册,境内企业达到72家,境外企业6家(其中惠氏被雀巢收购,美乐宝被纽迪希亚收购)
国产企业获批情况
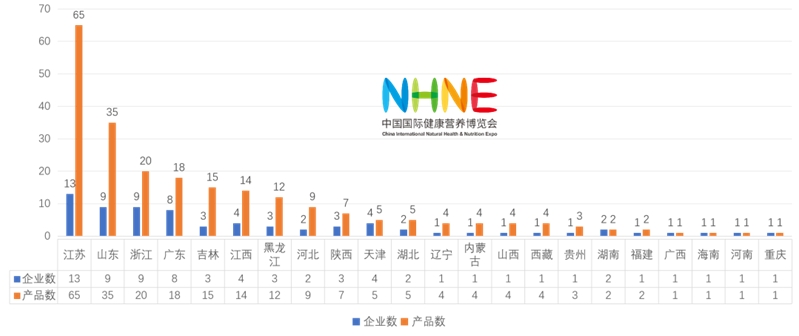
已获批国产232款特医食品中,所涉企业72家,分布在22个省市。获批情况分析如下:
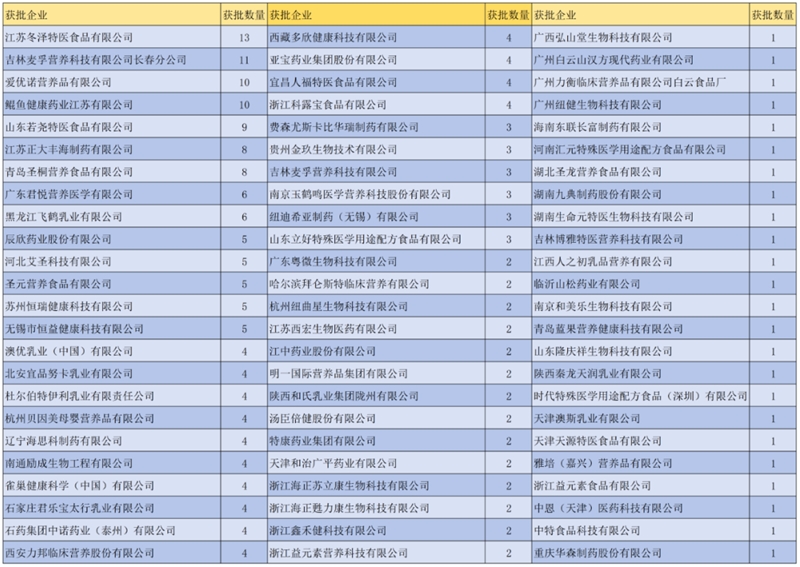
国产企业地域分布
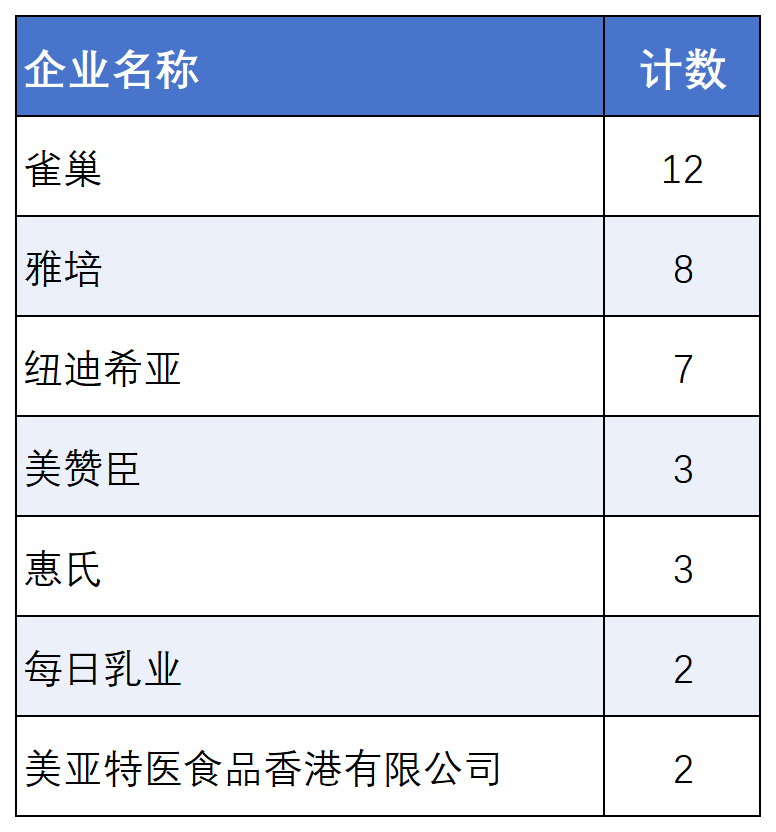
进口企业获批情况
2025年上半年,美亚特医获批2款香港首批特医产品
03
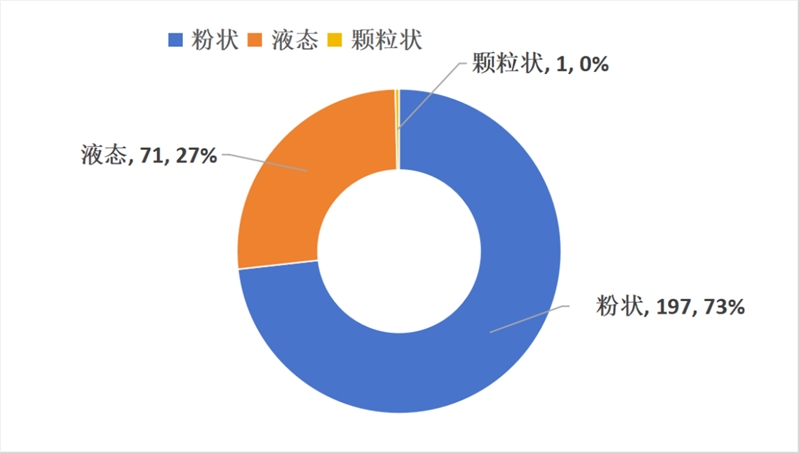
产品剂型分析
已获批的特医食品中粉剂197款,液态71款,颗粒状1款。无新增其他剂型,分布情况如下图:
04
总结分析
2025年上半年,我国特医食品行业迎来密集政策红利,国家多部门围绕临床试验标准、注册审评、应用场景拓展等关键环节推出一系列新规,旨在加速产业创新与规范化发展。从统计分析中可以看出,2025年上半年特医食品的获批数量延续了2024年的高增长趋势。
一、临床试验标准优化与扩容
1、新增两项临床试验指导原则
2025年5月26日,市场监管总局发布《特定全营养配方食品临床试验技术指导原则 肝病》和《胃肠道吸收障碍》,填补了这两类疾病特医食品临床试验的技术空白。文件统一了九大章节框架(如试验设计、观察指标等),取消样本量硬性要求,试验周期更具灵活性。
2、三项国标征求意见稿发布
2025年4月2日,糖尿病、肾病、肿瘤三类特定全营养配方食品的临床试验国家标准启动征求意见。相较于2019年版,新版删除“试验组有效例数不少于100例”的硬性要求,调整为“符合统计学要求”,并收紧试验方法(如糖尿病和肿瘤类仅接受随机对照试验)。
二、注册审评制度改革
1、分类注册指南完善
全营养配方:2025年初发布注册指南,简化材料提交(如免交配方设计依据、生产工艺设计依据等原始文件),明确仅三种情形需现场核查(如首次申请注册、生产线首次使用等)。
氨基酸代谢障碍类:同步发布注册指南,允许生产工艺相似产品豁免现场核查,降低罕见病特医食品研发门槛。
2、优先审评通道深化
临床急需产品(如罕见病类)审批时限缩短至30个工作日,加速填补供给缺口。
三、标准体系与标签标识规范
1、特医婴配新国标发布(GB 25596-2025)
2025年3月27日发布,新增生酮配方、防反流配方、脂肪代谢异常配方等6类产品,调整能量计算方式(如膳食纤维能量系数明确为8kJ/g),并将胆碱调整为必需成分。新标准于2027年3月实施,配套发布注册衔接问答。
2、标签标识统一要求
《食品标识监督管理办法》(2025年3月发布)要求特医食品集中标注六项核心信息(如适用人群、营养成分等),防止消费误导,2027年3月实施。
四、产业协同与支付创新
1、纳入国家健康消费战略
商务部等12部门《促进健康消费专项行动方案》将特医食品列为重点领域,鼓励企业加强创新,探索“医保+商保”支付模式(如南通试点商业保险报销)。
2、多部门联动机制强化
市场监管总局与国家卫健委建立“技术联动、专家联审”机制,对临床急需产品优先审评;推动特医食品纳入医疗机构HIS系统,破解“进院难”问题。
五、地方试点与场景拓展
1、江苏创新举措打通特医食品经营环节瓶颈堵点
2025年1月发布省级指导意见,选取三甲医院开展规范化试点(如纳入HIS系统),并在养老机构配备营养师推广个性化方案。无锡将特医食品暂纳入医保个人账户支付范围。
2、四川规范医疗机构管理
2025年1月出台《医疗机构特医食品经营使用管理办法》,要求医院成立特医食品管理委员会,明确处方开具、不良反应上报等流程,首次实现经营与临床应用的统一监管。
3、海南省发布先行区特医食品申报指南,明确申报要求,为特医食品在海南自由贸易港的临时进口提供了明确的操作路径和规范
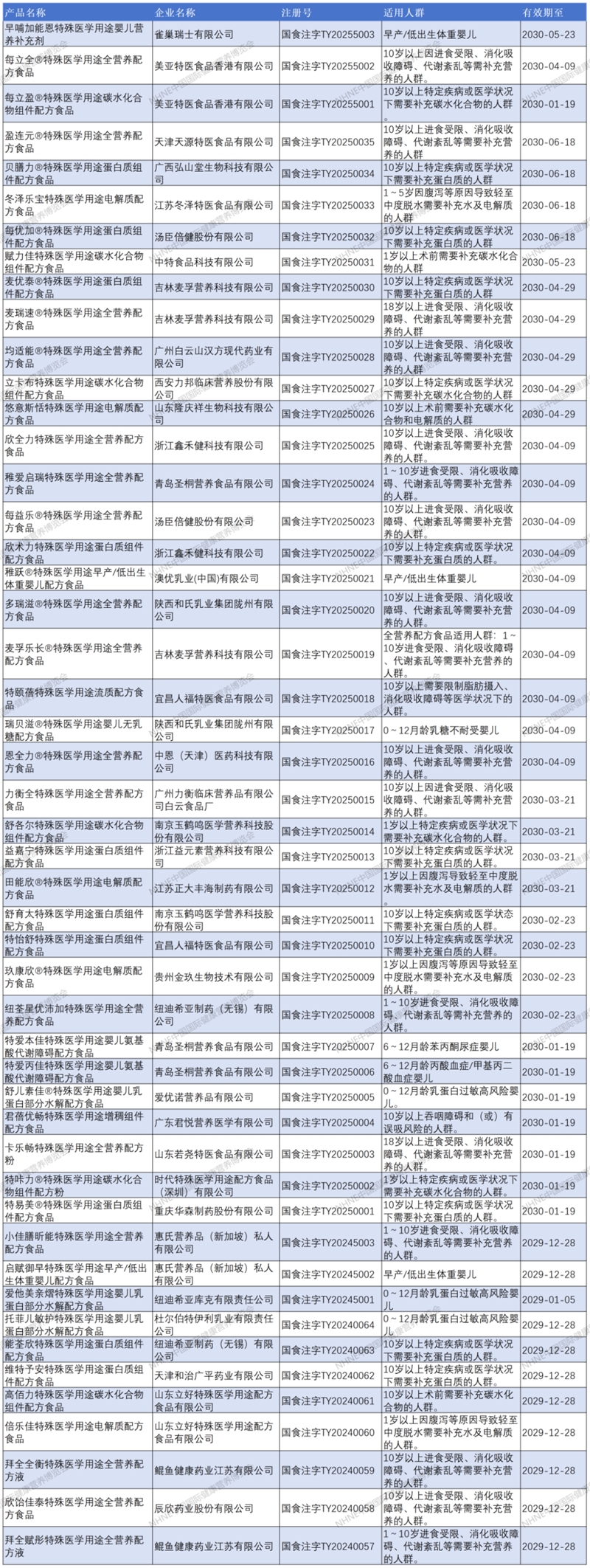
05
特医食品注册清单
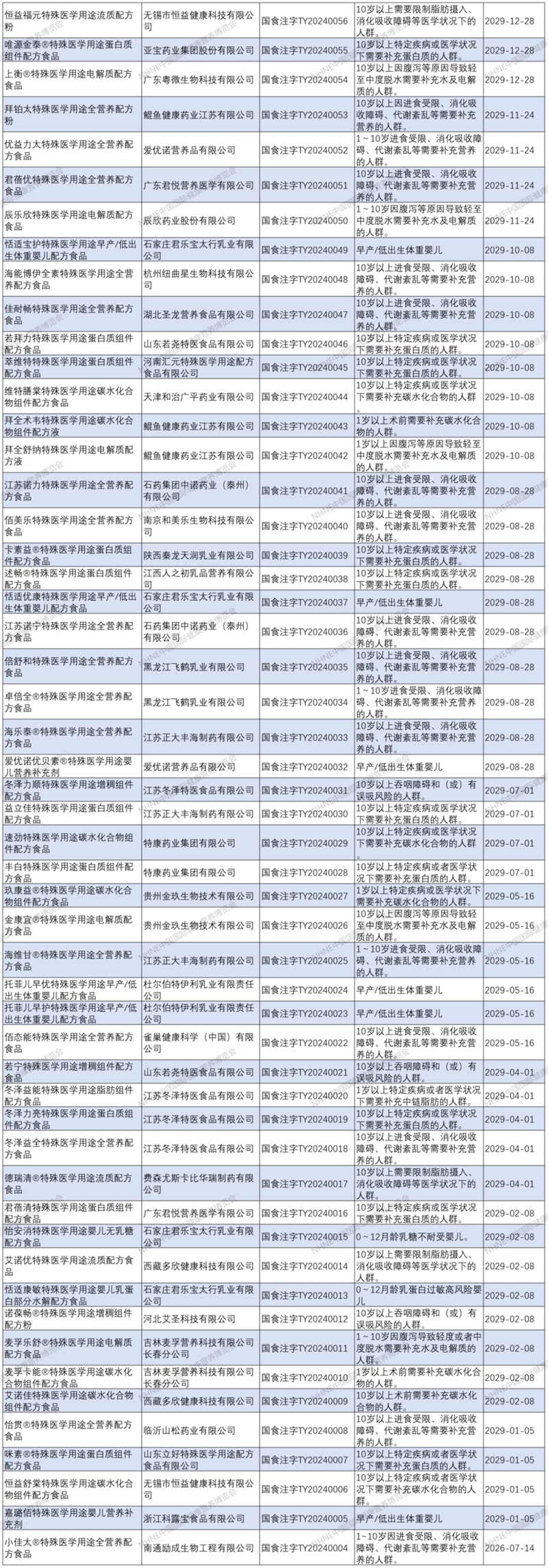

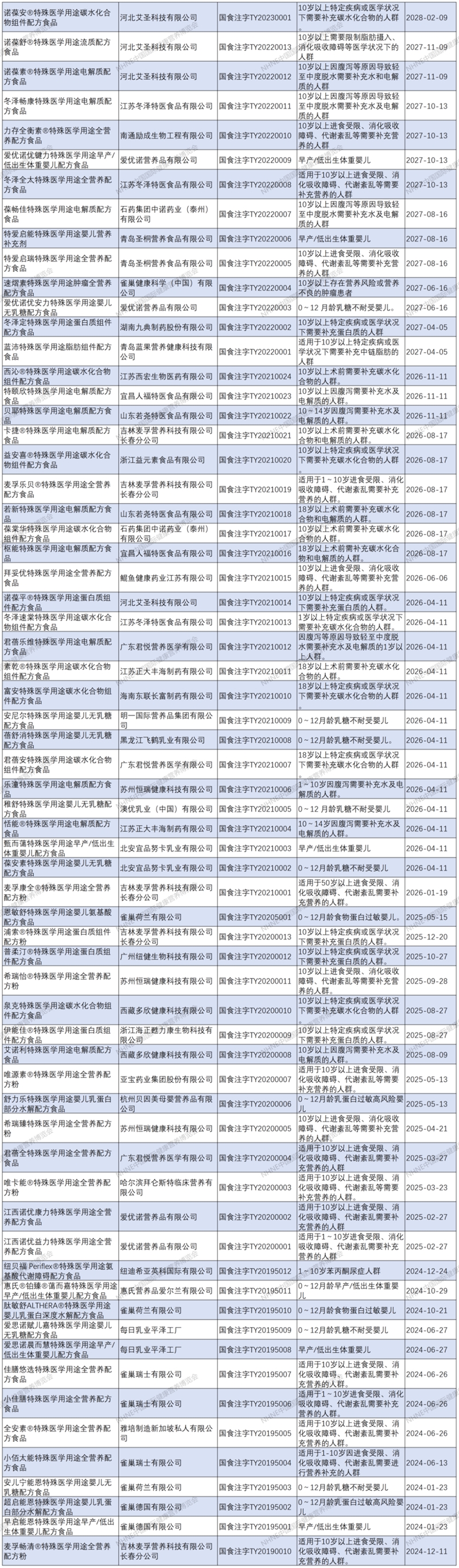
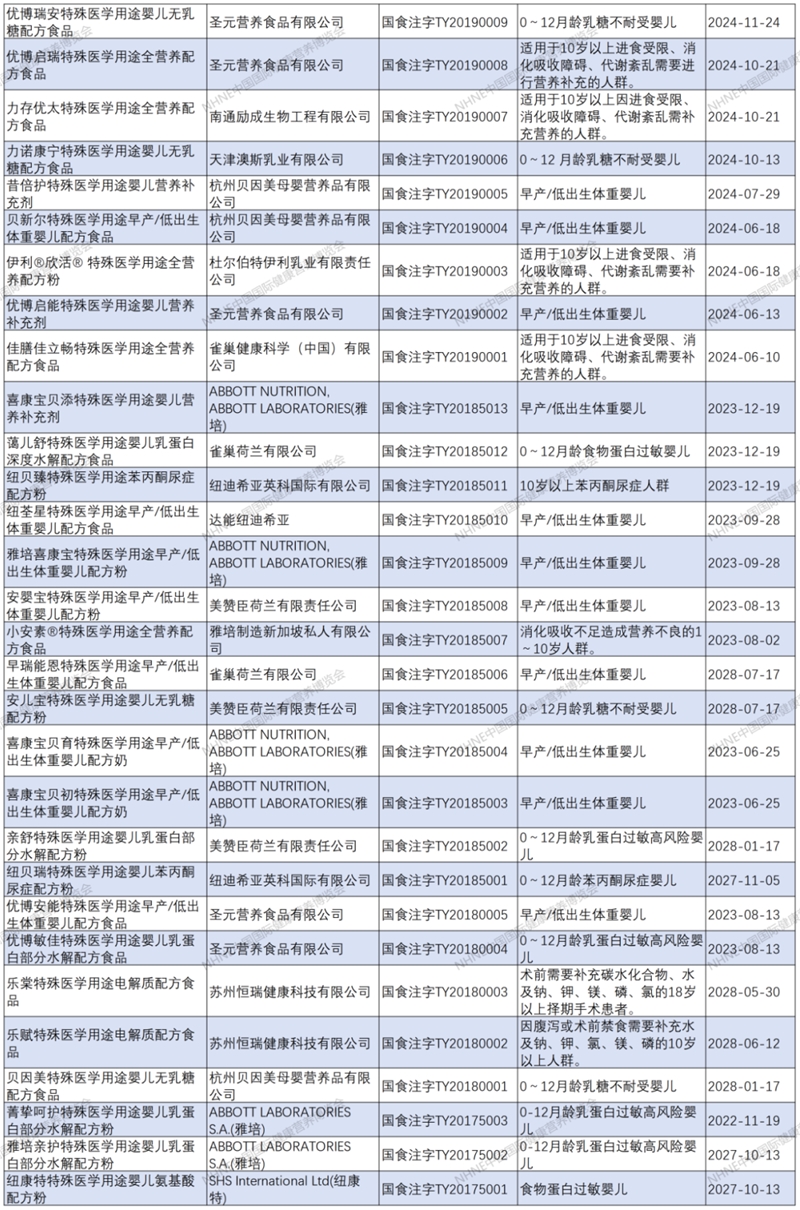
声明:转载此文是出于向母婴行业传递更多信息之目的。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。联系方式:168466559@qq.com



长按扫码 阅读原文


